Les molécules qui ont déjà été associées principalement à l’atmosphère ont été produites naturellement dans notre corps, jouant un large et sauvage assortiment de rôles. Par exemple, au milieu des années 1980 et au début des années 1990, le NO (oxyde nitreux), un polluant commun, a été démontré pour être synthétisé dans le corps à partir de l’acide aminé (arginine).

Modèle de l’acide aminé, l’arginine. Une enzyme NO synthase convertit l’arginine en citruline. L’atome de 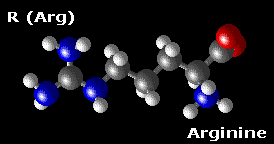 carbone marqué avec un C rouge a l’un de ses groupes amino (NH2) remplacés par un carbonyle. Le groupe amino est ce qui est oxydé au monoxyde d’azote.
carbone marqué avec un C rouge a l’un de ses groupes amino (NH2) remplacés par un carbonyle. Le groupe amino est ce qui est oxydé au monoxyde d’azote.
L’oxyde nitreux est un dilatateur des vaisseaux sanguins, ce qui permet à la chair molle du pénis d’engendrer  avec du sang et du champignon dans une forme rigide et fonctionnelle. Il agit également comme un neurotransmetteur dans certaines parties du cerveau, permettant le péristaltisme dans l’œsophage.
avec du sang et du champignon dans une forme rigide et fonctionnelle. Il agit également comme un neurotransmetteur dans certaines parties du cerveau, permettant le péristaltisme dans l’œsophage.
Au début des années 2000, les chimistes du Scripps Research Institute et d’autres ont découvert que les anticorps semblent catalyser la formation d’ozone (O3). Ils ont également montré que ce filtre UV stratosphérique important, mais le polluant au niveau du sol, est biosynthétisé dans les artères par des plaques athérosclérotiques. Dans le premier cas, les anticorps produisent d’abord la molécule H2O3 de courte durée, qui se décompose ensuite dans la réaction globale suivante:
H2O3 -> O2 + H2O2 + O3
L’ozone dans les systèmes aqueux est de courte durée, avec une demi-vie d’une minute, ce qui est probablement suffisant pour tuer les envahisseurs indésirables. La production de peroxyde seul ne suffit pas pour tuer les bactéries.
Vous remarquerez que la réaction globale ci-dessus n’est pas équilibrée.
Il existe plusieurs façons d’équilibrer l’équation sans créer de solutions redondantes.
n H2O3 -> xO2 + n H2O2 + y O3
3n = 2x + 2n + 3y
n = 2x + 3y
if x = y =1, then n = 5; if x = 2 and y = 1, then n = 7; etc…producing
5 H2O3 -> O2 + 5 H2O2 + O3
ou
7 H2O3 -> 2O2 + 7 H2O2 + O3
Il existe bien sûr de nombreuses autres solutions. Quelle est l’équation globale réelle? Peut-être qu’ils sont tous faux. Dans un article publié cette année, Arnold N. Onyango a soutenu que H2O3 se décomposait trop facilement dans l’eau pour former du singlet O2 et de l’eau plutôt que de O3 et H2O2. Il souligne que la littérature semble mieux soutenir une autre hypothèse. L’ozone peut avoir une origine acide aminé, analogue à la façon dont le NO est produit. Les progéniteurs pourraient plutôt être les acides aminés méthionine, tryptophane, histidine et cysteine. Lorsqu’il est oxydé par O2 dans un état à haute énergie (soi-disant singlet oxygène 1O2 or 1Δg ), de petites quantités d’ozone pourraient être produites.
the attachments to this post:

12771391-Amino-acid-arginine-structural-formula-Stock-Vector

225px-L-Arginin_-_L-Arginine.svg




